El remdesivir falló contra el ébola: ¿Qué tan efectivo es contra el Covid-19?
Universidad San Francisco de Quito
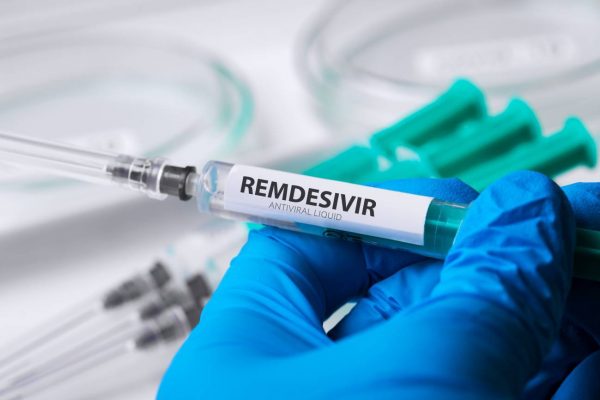
A inicios de mayo cuando se anunció que un medicamento había logrado tener un impacto en los pacientes con Covid-19 se generaron varias expectativas por dos razones: el costo y la adquisición del gobierno de los Estados Unidos del 90% de la producción para el manejo de sus pacientes. Se trata del remdesivir, un fármaco antiviral de la empresa farmacéutica estadounidense Gilead, cuyos primeros ensayos mostraron que podía reducir el tiempo de recuperación de los pacientes contagiados con el SARS-Cov-2.
El remdesivir como molécula pertenece a la familia de los antivirales, años atrás se lo creó para combatir el ébola, pero no tuvo éxito. Esta molécula fue un desarrollo en conjunto entre el laboratorio Gilead y el Departamento de Defensa de los Estados Unidos, sin embargo, debido a la alta mutación característica del virus del ébola, la utilidad del remdesivir se perdía rápidamente.
Pasaron los años y sobrevino el problema del SARS-CoV-2 y resultó que el remdesivir tenía actividad “in vitro” contra este nuevo agente y se propuso utilizarlo.
Sin lugar a duda, lo primero que salta a la vista es que se está intentando resucitar una molécula que no tenía utilidad para ninguna otra cosa.

El SARS-CoV-2 es un virus tipo ARN, es decir, indispensablemente necesita del material genético del ser humano para multiplicarse dentro del organismo. El remdesivir siendo un agente antiviral por definición, evita que el virus continúe replicándose y multiplicándose dentro del organismo, por lo que debería ser utilizado en los estados tempranos de la enfermedad. Pero si el producto se administra tarde, cuando la enfermedad ya ha avanzado, el efecto será menor y menos evidente que si se lo hace tempranamente.
Justamente, cuando se pregunta ¿cuál es la evidencia?, ¿cuál es la data con respecto al remdesivir en el Covid-19? tenemos otro problema importante, porque los estudios realizados han sido generalmente en pacientes con el estado de la enfermedad más avanzado, especialmente en hospitalización en las Unidades de Cuidado Intensivo (UCI) o con dificultad respiratoria. En esos pacientes, la única estrategia que ha logrado ser útil hasta ahora es el uso de corticoides, porque lo que conlleva a la muerte de un paciente con el nuevo coronavirus es una exagerada inflamación pulmonar masiva, que produce la dificultad respiratoria. La administración de corticoides disminuye la inflamación y por ende ayuda a los pacientes a reponerse.
En esos pacientes, el tratamiento con remdesivir ha permitido que se recuperen en 11 días, mientras que quienes no recibieron la molécula lo hicieron en 15 o 16 días. Es decir, el remdesivir no ha logrado disminuir la mortalidad, pero sí acelerar la recuperación del paciente.
Desde el punto de vista clínico esto es interesante, pero falta saber si hay una reducción en la mortalidad, por lo que existe un vacío de conocimientos en ese aspecto. Recién el día de esta entrevista salió publicado un estudio en pacientes con enfermedad moderada por Covid 19, el cual en definitiva tampoco muestra un beneficio en mortalidad en comparación al tratamiento estándar. Con estos antecedentes, uno se pregunta ¿por qué tanto revuelo con el remdesivir? y ¿por qué tanta presión sobre el uso? Una de las cosas fundamentales es que siendo una molécula liberada por un laboratorio de los Estados Unidos ha sido el principal foco de atención para la realización de las pruebas clínicas.
Y eso ha resultado incluso, en que se politice en cierta medida los resultados que se han ido obteniendo. Por ello, las declaraciones del presidente Donald Trump sobre la compra del 90% de la producción, para la población americana. Eso además de involucrar desconocimiento, genera un pánico generalizado porque la gente piensa que el producto no estará disponible, haciendo que las acciones de esta compañía se disparen, los precios suban y la demanda se imponga, de una forma exponencialmente más alta.
Pero, qué tanto nos beneficiaríamos de que el remdesivir venga al Ecuador y qué cantidad de pacientes lo van a necesitar? Haciendo un poco de numerología de lo que ya se sabe del SARS-CoV-2, al menos el 80% de los pacientes que dan positivo se curan únicamente con reposo, hidratación y algún analgésico o antiinflamatorio de uso doméstico. El 20% que se complicó necesita atención hospitalaria, de ese porcentaje al menos el 70% van a resolver los síntomas de una manera favorable y el 30% restante, de ese 20%, que son quienes se agravan van a terapia intensiva. Lastimosamente, la mayoría de quienes van a la UCI tienen una larga estancia o un desenlace negativo. Por ello, numéricamente de cada 100 pacientes, a las UCI llegan 5 a 6 y de ellos fallecen uno o dos. Si Ecuador va a traer el remdesivir, el 80% no será beneficiado, pero de ese 20%, ¿quiénes son los que obtendrán el medicamento? Acorde al conocimiento actual, son quiénes entran a terapia intensiva que representan un máximo del 10% de los pacientes. Tampoco hay la certeza que vaya servir como una terapia única o una adicional. El costo tiene un limitante importante, al menos en los Estados Unidos se ha reportado, oficialmente, que el valor del tratamiento con remdesivir, estimado en cinco días, será de alrededor de $3 000. En Europa el tratamiento por paciente bordea los €4 000, para el Ecuador no se sabe exactamente cuál sería el costo de adquisición. Hace un par de semanas hubo un desfase comunicacional, en principio se dijo que el Ecuador recibió una donación de 1 900 dosis del laboratorio estadounidense Gilead con apoyo de Biotoscana, para 320 pacientes. Luego el Ministerio de Salud Pública emitió un comunicado indicando que había gastado $70 mil. Nunca se especificó o se aclaró si el medicamento fue donado o comprado.
Lo cierto es que de parte del MSP, desafortunadamente, no existe una guía específica de utilización del producto, por lo cual podría ser asignado a los hospitales más grandes, eso aún no está definido. Eso si, tiene que establecerse qué medidas se van a instaurar para saber si es un producto útil o no, pues si sucede lo que hasta ahora, el MSP no tiene registro de qué pasa con el tratamiento que reciben los pacientes Covid-19 recuperados o no, y por tanto se seguirá simple y llanamente acorde a lo que la novelería indique.
Hay una gran probabilidad de que se produzca malestar en los médicos prescriptores y digan es que es fácil hablar desde los escritorios, cuando ellos están en primera línea tratando al paciente. Pero, justamente, atendiendo a esa sensibilidad, a esa solidaridad de los médicos que están frente a frente con el paciente se deben tomar decisiones fundamentadas. Ojalá con las 1900 dosis que están trayendo al país, se aproveche la oportunidad para documentar si es una estrategia útil y efectiva, si es que es beneficiosa en aras de tomar una decisión posterior mucho más adecuada.
Un medicamento condicionado
Siendo una molécula americana el remdesivir tiene que regirse por la normativa de la FDA, la Agencia Regulatoria Americana que viene a ser el equivalente a la Agencia Nacional de Regulación, Control y Vigilancia Sanitaria (ARCSA), aquí en el Ecuador. Esa normativa específica que, para que un fármaco sea aprobado tiene que tener al menos dos estudios de fase tres, que sean independientes, es decir dos estudios realizados por separado, no pueden estar vinculados entre sí. Si esos estudios no se presentan, la FDA no concede el registro sanitario, asimismo pone como condicionante, que la molécula no puede solicitar más de tres veces solicitud de registro sanitario.
Esta molécula remdesivir no cuenta con los dos estudios de fase tres, por lo cual no podría hacer la aplicación; sin embargo, por la emergencia sanitaria que se presenta y por la aparente eficacia que podría tener, a solicitud de las autoridades, especialmente del presidente Trump, la FDA está concediéndole una aprobación especial o condicionada para que se utilice única y exclusivamente para Covid-19. Eso significa que cuando la pandemia pase, no hay autorización para vender o comercializar el medicamento en los Estados Unidos. Para obtenerlo tendrá que volver a realizar todo el proceso.
Pero eso es un “artificio” legal americano, para permitir la comercialización del remdesivir en Estados Unidos. Por eso es muy preocupante, que el Ministro de Salud (Juan Carlos Zevallos), indique que se ha dispuesto realizar el trámite de registro sanitario en el Ecuador. ¿Por qué se va a dar el registro a una molécula que no lo tiene, en ningún otro lado? En su lugar, el MSP debería traer el remdesivir, como un medicamento excepcional, bajo la figura de un medicamento de emergencia.
Las vacunas
Con las vacunas caemos en el mismo problema, la angustia, que nos lleva a tomar decisiones equivocadas, porque en términos de vacunas lo más importante es determinar la duración de la inmunidad que puede proveer, junto con los problemas asociados a su uso o sus efectos adversos. Para determinar la seguridad de la vacuna se necesitan estudios a largo plazo. Hasta ahora ninguna vacuna va más allá de los tres meses y eso es gravísimo, porque si nos guiamos por los estudios significaría que hay que vacunarse cada tres meses y eso es imposible. Poco a poco se ha ido cambiado el discurso, en inicio se dijo que tendríamos la vacuna para septiembre, luego para el primer trimestre del 2021, otras dicen que con seguridad para el primer semestre del 2021, lo cual es más realista.
Sobre la vacuna anunciada por Rusia hay un hermetismo total en la información, no hay estudios publicados, ni datos disponibles, lo máximo que se sabe extraoficialmente es que han hecho lo mismo que las otras vacunas, es decir la fase uno y la fase dos. De forma similar, Rusia cambió por disposición de su presidente el proceso regulatorio y decidieron que, para registrar una vacuna no hace falta el estudio de fase tres, los más importantes. Pero eso no significa que esté probada, simplemente significa que tiene aprobación.
En todo caso, aún cuando tengamos en el mediano corto plazo una vacuna disponible, esta no va a tener efectividad inmediata; por lo tanto, no podemos deslindarnos de la autoprotección. Seguirá siendo indispensable el buen uso de la mascarilla, el distanciamiento y el lavado de manos frecuente, es un nuevo estilo de vida con el que debemos vivir en esta nueva normalidad.
¿Ya conoces nuestro canal de YouTube? ¡Suscríbete!













Realmente luego de leer a los analistas sobre esta pandemia, da ganas de suicidarse, nada funciona, todo está mal, nadie acierta…..sólo ellos